现场视频!瑞德西韦临床试验启动,首位受药的是68岁男性重症患者(视频/图)
2月6日晚,抗病毒药物瑞德西韦临床试验已在武汉金银潭医院启动。
据瑞德西韦临床试验项目负责人、中日友好医院副院长曹彬教授介绍,总计拟入组761例患者,采用随机、双盲、安慰剂对照方法展开。首位受药的是一位68岁的男性重症患者。

2月5日,中国工程院副院长、中国医学科学院院长王辰院士(右一)介绍项目情况。新华社记者 程敏 摄
备受期待的潜在抗疫新药瑞德西韦(Remdesivir),正式进入临床试验。
2月5日晚间,该药的生产商、跨国药企美国吉利德科学(下称”吉利德“)在回复时代周报记者采访时确认,目前,在武汉开展两项临床研究的瑞德西韦,是来自吉利德的自有库存。
“该药是一种试验性药物,迄今为止仅有极少数感染2019-nCov的患者使用过,因此我们对其疗效尚无足够充分的了解,且目前不足以确保药物能被广泛使用。“吉利德回复称。
当天下午,中日友好医院王辰、曹彬团队在武汉市金银潭医院宣布启动瑞德西韦治疗2019年新型冠状病毒感染研究,入组患者761例。
据介绍,此次临床试验计划入组轻、中症患者308例,重症患者453例,样本量超过此前网传的预计入组病患数。
中日友好医院教授曹彬表示,“这项研究将执行严格的随机、双盲试验,以评价瑞德西韦在新冠病毒肺炎的疗效和安全性。”
瑞德西韦是一种在研的广谱抗病毒药物,尚未在全球任何国家获得批准。
瑞德西韦在体外和体内动物模型中证明了对MERS和SARS病毒病原体的活性,它们也是冠状病毒,在结构上与2019-nCoV类似。
针对MERS和SARS有限的临床前数据表明,瑞德西韦可能对2019-nCoV具有潜在的活性。
就外界关心的瑞德西韦临床试验,吉利德回复时代周报记者采访称,“公司已与中国卫生部门达成协议,支持对2019-nCoV感染者开展两项临床试验,以确定瑞德西韦作为冠状病毒潜在治疗手段的安全性和有效性。”
其中,一项研究评估瑞德西韦用于确诊感染2019-nCoV且已住院但未表现出显著临床症状(如,需要额外吸氧)的患者的治疗效果;另一项研究则评估瑞德西韦用于出现较严重临床症状(如,需要吸氧)的确诊病患的疗效。
据悉,这两项临床试验由中国研究人员牵头,均在武汉进行。
吉利德无偿提供研究所需的药物,并为研究的设计和开展提供支持。
前述吉利德人士补充说,如果初步研究的结果表明瑞德西韦治疗2019-nCoV感染的潜在安全性和有效性,会通过适当的渠道将瑞德西韦这种试验性药物向更多患者开放。
此外,公司正与多家机构就未来临床试验的可能性进行讨论。
关于瑞德西韦的供应,是外界关注的焦点之一。
为了应对近年来在西非爆发的埃博拉疫情,吉利德扩大了瑞德西韦的生产,建立了产品库存应对未来的疾病大流行,同时增加了制造瑞德西韦的原材料库存。
考虑到当前情况的紧迫性,吉利德称,正采取多种措施加快生产进度,增加供应,包括拓展外部制药合作伙伴,以加快原材料的采购,原料药和药品的生产。
这家网站“瑞德西韦”10毫克售7650元 只卖给科研单位
作为治疗新冠肺炎的“希望”药物之一,Remdesivir(瑞德西韦)牵动着大家的心。
瑞德西韦为美国制药公司吉利德在研药物,截至目前,瑞德西韦尚未在任何国家获得批准上市,其安全性和有效性也未被证实。在美国首例新冠肺炎确诊病例的诊疗过程中,瑞德西韦作为“同情用药”使用后,患者病情出现了迅速缓解。基于此,瑞德西韦也被认为是治疗新冠肺炎的潜在有效药物。
《每日经济新闻》记者注意到,一家名为“美国GLPBIO中文站”(以下简称GLPBIO中文网)的网站上,有多种规格的瑞德西韦出售。从单价来看,这批产品的售价堪称惊人。
GLPBIO中文网显示,其售卖的瑞德西韦规格有5种,分别为10 mM*1 mL in DMSO、5mg、10mg、50mg、100mg。前三种规格的售价分别为6562元、4950元、7650元,库存显示为“现货”,后两种规格的价格和库存均显示为“询价”。
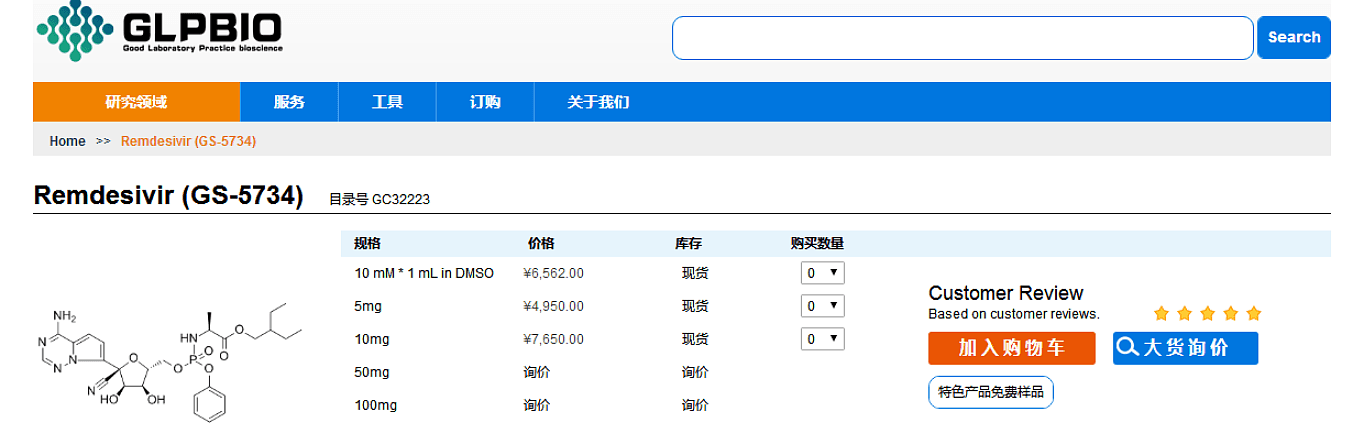
图片来源:网站截图
根据网站的产品介绍,瑞德西韦是一种核苷类似物,具有有效的抗病毒活性,在HAE细胞中,对ARS-CoV和MERS-CoV的EC50值为74 nM;在延迟脑肿瘤细胞中,对鼠肝炎病毒的EC50值为30 nM。
2月6日晚间,《每日经济新闻》记者以意向购买者身份拨打了网站上的销售电话,接电人士表示:“我们的产品不对个人提供,购买者必须是科研单位。”
对于瑞德西韦对新冠肺炎可能有效的情况,上述人士表示:“明白,但我们卖的这个产品不是药,是用于科研项目的。”对于产品是否由吉利德提供,该人士称:“不是,我们做科研研发用的。”
据网站介绍,GLPBIO创立于2016年,总部设在美国加州Montclair,公司主要客户包括世界各大制药厂、生物科技公司、医院及各大临床诊断试验室等。GLPBIO的产品涵盖癌症、神经科学、抗感染、表观遗传学等20个热门研究领域,覆盖Akt、Jak等近千个细分靶点。其中国公司位于上海市杨浦区长阳路。
目前,吉利德的瑞德西韦在中国的临床试验在加快推进中。
2月2日,中国国家药监局药品审评中心(CDE)受理瑞德西韦的临床试验申请。据吉利德对外披露,在武汉进行的临床试验有两项,一是研究评估瑞德西韦用于未表现出显著临床症状患者的治疗效果,也就是轻、重症患者。另一项则是评估其用于重症确诊病患的疗效。
临床试验牵头方中日友好医院方面披露的细节显示,上述临床试验将入组患者共761例,其中轻、中症患者308例,重症患者453例。这些病例将执行严格的随机(患者吃的药物按安慰剂组、全量组、半量组等随机发放)、双盲(医生和患者均不知道患者服用的是药物还是安慰剂)试验。
华夏时报报道称,2月6日,瑞德西韦在完成临床试验的注册审批后已运抵抗疫一线,正式被用于武汉金银潭等一线医院首批新冠肺炎患者治疗。
值得一提的是,网络上近来流传着一张有关瑞德西韦的“进口药品通关单”。单据显示,这批药物从北京入关,总共2843盒,每盒一支注射剂,其中有150毫克药物。进口的价格为56465美元,报关价20美元一盒。不过,该通关单的真实性未得到官方证实。
而据华夏时报报道,吉利德无偿提供临床试验研究所需的药物,并为研究的设计和开展提供支持。
专题:武汉爆发新冠肺炎进入专题 >>
李文亮医生五周年忌,海内外网友悼念,吁言论自由(组图)
白宫:新冠病毒源自中国实验室是“可证实的事实”(图)
李文亮逝世五周年!父母痛诉:未能见最后一面(视频/组图)














 +61
+61 +86
+86 +886
+886 +852
+852 +853
+853 +64
+64


