在中国卖70万一针的救命药,在澳洲只要205元!真相到底是什么?(组图)
罕见病脊髓性肌萎缩症(SMA)及其治疗药物诺西那生钠注射液,顾名思义,原本都是罕见的名词,近日却在一则申请消息的发酵下登上微博热搜。
据相关报道,一种治疗罕见病脊髓性肌萎缩症(SMA)的特效药诺西那生钠注射液,一针售价69.7万人民币,每年需反复注射且完全自费,有的患者还需终身注射。但有网友透露,该药在澳洲仅售41美元(约合人民币205元)。
在看到一则针对诺西那生钠注射液的求药消息后,广东一位母亲向国家药品监督管理局提交信息公开申请,希望了解诺西那生钠注射液的采购方式和国内定价依据。
8月6日,#医保局回应一针药卖70万#冲上微博热搜榜首。

70万元和205元的天差地别,让舆论哗然。但这样的对比是否属实、合理?到底是什么原因导致了如此夸张的差价?是否如部分媒体评论所称存在“何其狠也”的中间商?类似诺西那生钠这样的“天价救命药”,又能否纳入医保,给予更多患者生的希望?
01
“天价”救命药
7月31日,一家名为“黑土影像”的自媒体发布一篇题为《湖南一男婴ICU中急需特效药救命,5毫升70万元,父亲瞬间绝望》的文章,写到一名男婴出生不久即患上脊髓性肌萎缩症(SMA),要想活下去则必须使用特效药诺西那生钠注射液。可近70万元一支的“天价”,让男婴一家濒临绝望。

随着文章广泛传播,男婴一家的境遇引起无数网友心疼叹息,文内提到的“天价”特效药诺西那生钠也进入大众视野。而引人关注的是,有网友指出诺西那生钠在国外的售价并不贵:在澳洲只卖41美元,相当于人民币200多元。如此大的价格反差引来众多网友质疑。
公开信息显示,脊髓性肌萎缩症(Spinal Muscular Atrophy,SMA) 是一种罕见的遗传性神经肌肉疾病,在新生儿中发病率约为1/6000-1/10000。根据起病年龄和运动里程的获得情况,SAM分为SMA-I型、II型、III型和IV型,如果不进行治疗,大多数SMA-I型的患儿无法存活到两岁。
在诺西那生钠注射液上市之前,此病无药可治,国内及全世界范围内对SMA的治疗措施仅限于呼吸支持、营养支持、骨科矫形等辅助治疗。
据悉,诺西那生钠注射液由渤健公司(Biogen Idec Ltd)研发,2016年12月23日首次在美国获批,是全球首个SMA精准靶向治疗药物,随后在欧盟、巴西、日本、韩国、加拿大等国家相继获批。2019年4月28日,诺西那生钠注射液在中国上市,用于治疗5qSMA,并成为中国首个治疗SMA的药物。另外两种治疗SMA的药物,罗氏的Risdiplam和诺华的Zolgensma均未在国内上市。
02
在国外售价同样高昂
据《正解局》报道,一边是70万,一边是205块,相差超过3400倍!
很多网友很愤怒:这完全是把人往绝路上逼。
还有人专门向有关部门申请信息公开,想弄明白这个药在中国为什么卖得这么贵?
结果也没搞清楚。
颇有几分叫天天不应的味道。
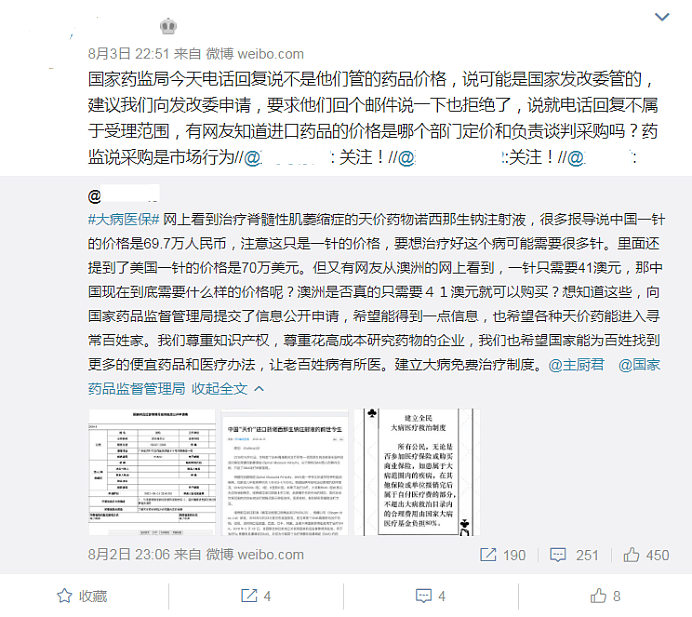
少不了有人开始带节奏。
03
自费药和医保药
真相到底是什么?
这个药是美国百健(Biogen)和Ionis制药公司合作开发的,也是美国FDA批准的第一种治疗儿童和成人脊柱肌肉萎缩症的药物。
实际上,在这个药物推出时,纽约时报就评价,这是世界上最昂贵的药之一。
在美国,打一针要12.5万美元,合人民币86.7万元。
第一年,要打五到六针,也就是要花62.5—75万美元。
以后,每年要打3针,花费37.5万美元。
而且,可能要终生用药。
也就是说,美国治疗第一年要四五百万元人民币,后面每年还要花260多万元人民币。
可见,美国用药并不比中国便宜。

那为什么中国、美国那么贵,澳大利亚却那么便宜呢?
简单来说,就是医保。
澳大利亚这种药卖41澳元,是加入了医保的价格。
实际上,这个药发行价高达11万澳元,将近55万人民币。
还有网友透露,在日本这种药还是免费的,其实无外乎也是因为纳入了医保,由医保买单。
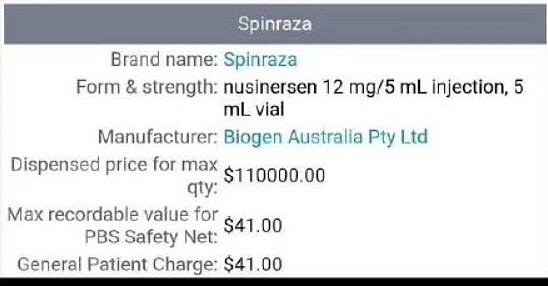
实际上在澳大利亚这个药仍然是天价
那么,问题来了,为什么澳大利亚、日本能把药纳入医保,中国就不能呢?
根据网上一个平台统计,目前全世界只有14国家(地区)对这个药可以完全报销:
奥地利、比利时、法国、德国、意大利、卢森堡、波兰、葡萄牙、罗马尼亚、苏格兰、以色列、土耳其、中国香港、日本。
至于澳大利亚,这个平台显示,是针对18岁以下未成年人有报销。
这也是目前大部分国家的做法:只给未成年人报销。
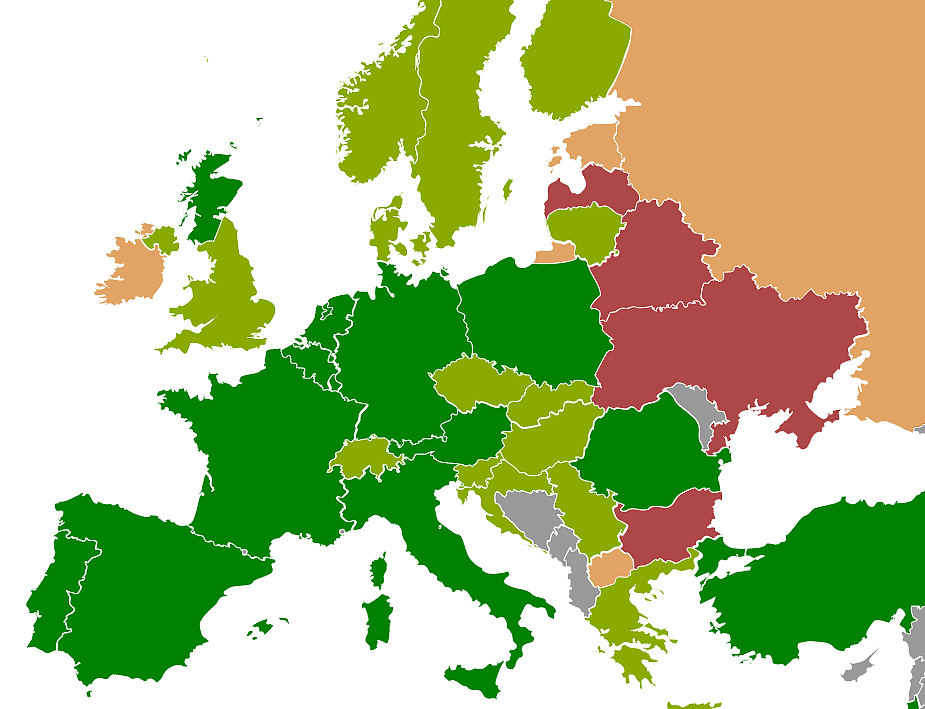
深绿代表完全可以报销,浅绿代表有限制的报销,浅红代表正在进行价格谈判,深红代表还处在进入的前期
实际上,哪怕是在很多发达国家,也没有把这款神药纳入医保。
比如,丹麦只同意给婴儿使用,不能作为其他患者的标准疗法。
挪威开始不同意使用,在2018年2月批准只用于18岁以下的未成年人。
原因只有一个:太贵了!
这也就是现实残酷的地方:药企冒着巨大风险研制出药物就是为了赚钱,针对的又是罕见病,量上不去,单价肯定要高。
但如果医保买单,那将是一笔巨额的开支。
上面这些全部报销的国家里,每年出生人口最多的是德国,也不过是80万左右,也就说大概只有80个新生儿会得这种病。
但中国是1500个左右,将近德国的20倍。
按照美国的行情,第一年每人花费四五百万人民币,后面每年260多万人民币。
累积下来,就是一个庞大的数字。
要知道2019年,中国全国职工医保次均住院费用才不到1.2万元。
其实,财富从来不会凭空来,资源总是有限的。
据渤健声明,近年来,中国陆续出台一系列政策,加速罕见病药物审批,提高罕见病患者用药保障,SMA这一罕见疾病率先受益于国家罕见病相关政策。
2018年5月,SMA被纳入国家《第一批罕见病目录》。
2018年11月,诺西那生钠注射液被列入《第一批临床急需境外新药名单》。
2019年2月,诺西那生钠注射液通过优先审评审批程序在中国获批。
诺西那生钠注射液目前在中国属于自费药物。渤健表示,深刻理解应对支付挑战对中国SMA患者群体的重要性和迫切性。2019年5月31日,中国初级卫生保健基金会宣布SMA患者援助项目正式启动,帮助SMA患者第一年的治疗费用相比全自费节省约2/3,之后每年的治疗费用与全自费相比可节省约一半,援助药物由渤健公司捐赠。截至目前,全国已有80多位SMA患者在援助项目的帮助下获得了药物治疗。
然而根据国家相关规定,参加2019年国家医保谈判的药品必须是2018年12月31日前获得批准的药品。诺西那生钠注射液于2019年2月获批,不符合参加2019年国家医保谈判的条件,因此并未参加2019年国家医保谈判。渤健一直与国家和地方政府相关部门保持积极沟通,呼吁建立多方共付机制,以进一步提升中国SMA患者药物可及性。
04
复杂的罕见病保障体系
“这个新闻里的价差,是将个人自付费用和药品总费用混为一谈。”上海市卫生和健康发展研究中心主任金春林在接受21新健康采访时解释,这个事件引发关注,“一是反映出中国医疗保障制度覆盖率尽管已达到95%以上了,保险覆盖的宽度和强度还非常脆弱,老百姓大病负担仍然很重;二是不能一味苛责药企,罕见病的病人少,研发成本高,要回收研发成本均摊到每个患者身上的钱就贵。”
他表示,“应该用国家风险分摊的方法去解决这个问题,用全国人口的大数法则提高特病医保统筹层级至国家级,进行筹资和风险分摊,国家层面建立罕见病专项保障制度显得非常紧迫和重要。”
8月6日,IQVIA艾昆纬中国管理咨询执行总监李扬阳在IQVIA中国罕见病医疗保障论坛上表示,回顾过去10年中国在罕见病的历程,依然面临三个保障难题。第一是药物的可获得性上依然有很大的缺口;第二是对于罕见病的医疗保障,依然缺乏全国层面的制度化设计,同时一些超高值的罕见病药物在医保上没有实现0的突破;第三是罕见病的医疗保障在不同区域之间、不同省市之间存在非常大的挑战。
“过去3年,国家医保谈判中陆陆续续纳入越来越多罕见病的药物,尤其是2019年历史性第一次有超过11种罕见病药物进入国家医保,3种纳入国家医保类,8个通过谈判纳入。但回到现实层面,进入到国家医保药物目录的还只是少数,中国只有35种罕见病相关医疗药物,63个治疗药物已经上市,但目前只有21种罕见病、38个治疗药物被纳入到国家医保目录里,意味着还有非常多罕见病药物没有被纳入医保。”
要解决罕见病的支付问题和背后的保障体系,需要先了解这些不罕见的“罕见病”。
由于发病率很低,罕见病又称为“孤儿病”。“玻璃人”(血友病)、“木偶人”(多发性硬化症)、“不自觉跳舞”(亨廷顿舞蹈症)、“松软儿”(脊髓性肌萎缩症)等都是罕见病。
2014年,美国发起了一项为罕见病“渐冻人”(肌肉萎缩性侧索硬化症)捐款的“ALS冰桶挑战”公益活动,让罕见病逐渐为大众所知晓,从政策、药物、医疗保障体系等多方面推动了罕见病行业发展。

2014年8月,姚明完成ALS冰桶挑战
EURORDIS在2008年发起并确定了2月29日为国际罕见病日,四年一次的日子意寓罕见病之“罕见”,后将每年二月的最后一天定为国际罕见病日。
罕见病不是单一一种疾病,各国对罕见病的定义和标准不一:在美国,罕见病是患病人数低于20万人的疾病;在欧盟是患病率低于1/2000的疾病;在日本则是患病人数低于5万人或总病患数18万人以下的难治或顽固性疾病。
中国大陆对罕见病还没有正式的定义,但本地医学专家普遍接受以新生儿发病率万分之一、其他疾病患病率50万分之一作为分界点。由于流行病学相关研究稀少,政策中规定的任何数字分界在很大程度上都是有待商榷的。
全世界已知的罕见病约有7000种,按照五十万分之一发病率测算,预估中国罕见病患者总数不低于2500万。
2019年2月23日,中国财政部等四部门发布了《关于罕见病药品增值税政策的通知》,决定从3月1日起,对首批21个罕见病药品和4个原料药,国内环节可选择按照简易办法依照3%征收率计算缴纳增值税,进口环节减按3%征收增值税,是为罕见病的减税利好政策。
大多数罕见疾病都是遗传性疾病,即使症状没有立即出现,也可能会伴随一个人的医生。EURORDIS数据称,个别罕见疾病可能只影响一百万人中的一人,但所有罕见疾病患者共占欧盟人口的6%至8%。
05
罕见病的多重困境
罕见病面临一系列不罕见的问题也已是业界共识。
由于罕见病本身的特殊性,单个罕见病病种,无论在新药研发还是临床治疗方面都面临着诸多挑战。很多罕见病认识水平低、误诊率高、药物可及性也很差;罕见病药物公司也面临着投入高、研发难、上市难的风险;对于一些罕见病病种患者来说,无药可医、有药价高、难进医保、甚至进了医保可能也买不到药都是“常态”。
罕见病的首要困难是难诊断。以上面提到的脊髓性肌萎缩症(SMA)为例,这是一种被称为“2岁以下婴幼儿头号遗传病杀手”的罕见病,患者脊髓内的运动神经细胞受到侵害后,会逐渐丧失各种运动功能,包括呼吸和吞咽。
很多儿科医生都对它知之甚少,甚至有些神经科医生也不一定能做出准确诊断,导致误诊率居高不下。一旦不幸确诊,患儿和家庭还将继续面临无药可用的窘境,只能从护理和营养上维持和改善患儿的器官功能。
根据经济学人智库(EIU)发布的《无声的苦难:亚太地区罕见病的认知与管理评估》报告,500多名临床医生对调查所提到的全部18个医疗服务要点皆经常感到挑战,其中最大的问题是诊断,不仅要辨认出正确的病因,更要在合理时间内确诊。将罕见病诊断及管理列为国家罕见病政策要解决的首要问题。
来自美国的数据显示,从出现症状到最后确诊一种罕见病,平均需要4.8年;澳大利亚2016年一项调查显示平均确诊时间为4.7年,期间平均咨询过五名不同医生。
在诊断罕见病效率方面,明显障碍是世界上6000多种罕见病当中,有许多病症仍然缺乏可靠的检测方法来辨识。
其次的困难是“无药可用”。
治疗罕见病的药物又叫孤儿药,由于患者太少,在正常市场条件下,无法靠销售回收前期高额的研发投入,制药公司对开发仅针对少数患者的产品几乎没有兴趣。
此前在第七届中国罕见病高峰论坛上,国家卫健委罕见病诊疗与保障专家委员会副主任委员丁洁表示,一方面,对罕见病发病机制研究不足,对治疗靶点的研究也不够;第二,企业对罕见病药物的开发动力不足;第三,由于患病人群少,难以找到足够数量的病人开展相关临床试验,无法满足药品上市的要求。
对此,各国在孤儿药的研发上都作出了不同程度的鼓励,美国在1983年通过的孤儿药法案对其研发进行了经济激励,包括研发成本的50%税收抵免、孤儿药专营权排他性条款等,进而影响了日本在1993年、欧盟在2000年制定了相关政策。
“中国罕见病整体行业发展起步比较晚,政策上现在还没有一部全国性的罕见病法规。”罕见病发展中心(CORD)创始人、主任黄如方此前在接受21新健康采访时表示,2009年之前,罕见病在国内是被忽视的状态,“09年我们引入了罕见病日、做了大量宣传;2009年至2014年期间,是罕见病被广泛关注的时期,孵化出了大量罕见病患者组织,临床专家也越来越正视罕见疾病患者群体。”
但公众仍然对罕见病有一些误区,如觉得离自己很遥远而不关心,患者太少可以忽略,“还有一些误解觉得罕见病药物都特别贵,一个病人占了很多医疗支出,但罕见病人首先面临的是无药可医,有药用了不能用价格来衡量,应该是用价值来衡量。每一个人都应该有基本的医疗保障,在价格问题上可以通过多方努力去解决。”
2014年出现了冰桶挑战赛,让渐冻人成为最为著名的罕见病病种。仅在美国就有170万人参与挑战,250万人捐款,总金额达1.15亿美元,这可能是为某种疾病或紧急情况捐助最多的款项。
2015年,中国成立了罕见病专家委员会,“从15年到现在是政策陆续出台的阶段,我乐观估计到2020年,罕见病产业会得到较大的发展。”
2018年4月,国家卫生健康委员会等5部门联合制定了《第一批罕见病目录》,包含121种罕见病。据不完全统计,仅44个病种有相关药物在全球上市,多数疾病还处于无药可治的状态。10月,药监局发布罕见病防治医疗器械注册审查指导原则。包括依库珠单抗、艾美赛珠单抗等多个罕见病药物加速获批上市。2019年2月,国家卫健委发布了建立全国罕见病诊疗协作网的通知。
“能看出国家对于罕见病问题、特别是患者临床用药是下了决心要解决的。”黄如方说,“督促各个部委如卫健委、药监局、科研系统、医保部门陆续出台一系列政策。”
黄如方认为,可以预见到的是,未来几年,“一是国外的罕见病药物将会井喷式进入中国市场,特别是国家目录里相对应治疗的疾病。二是会激励中国医疗产业对于罕见病药物的防治和创新研发。三是加快罕见病患者的诊断、更加规范的治疗。四是解决患者可及可负担问题,医保部门会在罕见病药品的报销有更明确的举措。”
06
“天价”药物们有希望纳入医保吗?
罕见病药物罕见,价格自然也金贵。
EvaluatePharma《OrphanDrug Report 2018》数据显示,预计从2018年到2024年,全球孤儿药销售将以11.3%的复合年增长率增长,是非孤儿药市场6.4%的两倍;预计到2024年,孤儿药将占全球处方药销售额的五分之一,达到2620亿美元。
尽管最近两年孤儿药的定价增长有所放缓,但2017年,每位患者的平均成本仍然达到了147308美元,是非孤儿药的平均成本30708美元的四倍多。
由此吸引进入行业的玩家也越来越多。2019年1月8日,武田制药完成对罕见病公司夏尔(Shire)的收购,交易金额约624亿美元。
罗氏中国神经学领域临床科学家张巍峰此前在罕见病论坛上表示,2017年罗氏研发总投入106亿美元,其中相当一部分投在罕见病领域。“目前进入临床研发及上市阶段的罕见病药物总共9个,覆盖超过10种罕见病,已经完成和正在进行的临床实验超过50项。”
但除了研发,罕见病药物的准入、上市后如何提高可及性也是难题。
张巍峰表示,“当临床实验的结果交到国家药品监督管理局的时候,由于这些数据相对比较贫乏,不像糖尿病、高血压有几万人的数据,罕见病一般只有几十人的数据。要做出一个有效、正确的判断,本身也是一个困难的过程。”
在美国,“很多小型生物制药公司在罕见疾病药物的研发前期阶段,会得到非常多的公共资源支持。”黄如方介绍,如果没有政策优惠,研发难以为继,美国最大的亨廷顿舞蹈症基金会每年投入数千万美元进行科研,“很多钱都是打水漂的,亨廷顿舞蹈症现在仍然没有治疗药物,基础研究一定需要公共资源去投入。罕见病产品到临床阶段才可能挣钱。欧美很多小的孤儿药公司当药物到临床阶段就卖给大公司。中国现在非常薄弱的环节是公共资源的投入非常少,到底能募集到多少公共资源去投入到药物前期研发阶段,我们自己也在思考这个问题。”
另外,也会出现一些“中国特色的问题”,比如一些药物进入国内后没有相应的罕见病适应症获批;进了医保但在医院买不到药,黄如方说,“比如对于药占比的过度考核导致很多罕见病药物在一些医院买不到;一些疾病需要门诊治疗,但是政策规定可能住院治疗才能报销。”

针对诺西那生钠注射液未能进入医保,据红星新闻,国家医保局信访办一工作人员表示,该药物价格是由药企自行定价,所以在每个国家的价格存在一定出入,“除了药物的原材料、研发成本等,药企业也会考虑利润问题,加上该药物目前在国内处于市场垄断的情况,价格也一直居高不下。”
该工作人员表示,诺西那生钠注射液自2019年在国内上市以来,已被纳入医保谈判日程,国家希望和相关药企业谈判,将药物价格降下来,进而满足SMA患者的需要。“去年开始国家就在和药企谈判,由专家组研究定价,具体定价多少不清楚。但是纳入医保的事没有谈下来,因药物价格下不来,就始终没办法进入到医保目录。”上述工作人员表示。
为何药企价格不下降,就无法纳入医保呢?该工作人员进一步解释称,由国家医保局制定的医保目录适用于全国各地,因此需确保进入医保目录的药各地方都能用得起。“此类罕见病药物一旦纳入医保目录后,对于欠发达地区来说,基金用于支付高价罕见病后,其他基础疾病可能保障不了,后续还可能会造成地方经济压力,所以最根本的解决方式就是国家和药企谈判,将价格谈下来。
对于罕见病救助和保障,目前中国各地方政府也在因地制宜地摸索出各种特色模式。中国药促会医药政策委员会副主任刘军帅介绍,很多地方已探索出很多模式,如浙江模式、青岛模式,都是由当地政府主导,部分病种多方共付的模式,具有政府多部门联动、社会多方资源共享的特点,患者在报销后,自付的费用在承受范围内,最大程度减轻患者经济负担。
“医疗保障制度最关键在于公平和可持续。”刘军帅认为,一方面可以将社会保险与慈善相结合,提高罕见病药报销比例;另一方面,针对罕见病医保报销制定出独立的罕见病政策,单独筹资单独支付。医保三大要素,筹资、待遇、付费,三者均需独立。“罕见病医疗保障是一个伦理问题,少数人的生命也是生命,所以必须给予良好的福利政策;但是,如果与其他病放在同一个体系里,公平性问题必然绕不开,所以需要独立筹资独立运作。”









 +61
+61 +86
+86 +886
+886 +852
+852 +853
+853 +64
+64


